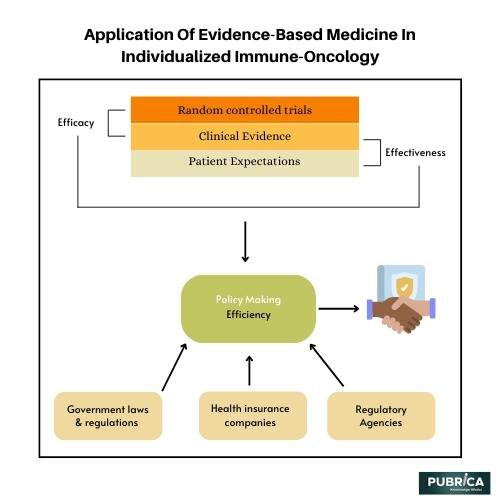
ایمونوتراپی به عنوان یک رویکرد نوآورانه برای درمان سرطان ظهور کرده است، اما اثربخشی آن بین بیماران بسیار متفاوت است. بار جهش تومور (TMB) به عنوان یک نشانگر زیستی پیش بینی کننده بالقوه برای پاسخ به ایمونوتراپی پیشنهاد شده است. این مطالعه با هدف انجام یک متاآنالیز و بیوانفورماتیک ارزیابی نقش TMB در پیش بینی اثرات ایمنی درمانی در انواع مختلف سرطان از طریق بررسی جامع ادبیات موجود و ادغام مجموعه دادههای ژنومی در مقیاس بزرگ، هدف ما روشن کردن رابطه بین TMB و نتایج ایمونوتراپی است. یافتههای ما ممکن است به اصلاح معیارهای انتخاب بیمار برای ایمونوتراپی و توسعه استراتژیهای درمانی شخصی کمک کند.
معرفی
خرچنگ یکی از دلایل مهم مرگ و میر و یک مانع بزرگ برای افزایش امید به زندگی است و موارد جدید تقریباً در همه کشورهای جهان در حال افزایش است. جراحی، پرتودرمانی، شیمی درمانی و درمان هدفمند مدتهاست که به عنوان رویکردهای اولیه برای درمان سرطان شناخته شدهاند. توسعه ایمونوتراپی درمان سرطان را تغییر داده است. چندین پیشرفت قابل توجه در درمان سرطان با استفاده از مهارکننده های ایمن ایست ایست ایست (ICIs) ایجاد شده است.
ایمونوتراپی که از توانایی سیستم ایمنی برای هدف قرار دادن و از بین بردن سلول های سرطانی استفاده می کند، انقلابی در درمان سرطان ایجاد کرده است. با این حال، موفقیت آن در دستیابی به پاسخهای بادوام در بین بیماران متفاوت است و نیاز به نشانگرهای زیستی پیشبینیکننده قابل اعتماد را برجسته میکند. بار جهش تومور (TMB)، تعداد کل جهش ها در ژنوم تومور، به عنوان یک شاخص بالقوه پاسخ ایمونوتراپی توجه را به خود جلب کرده است. نقش TMB در پیش بینی ایمونوتراپی اثرات، اگرچه امیدوارکننده است، اما همچنان موضوع تحقیقات در حال انجام است.
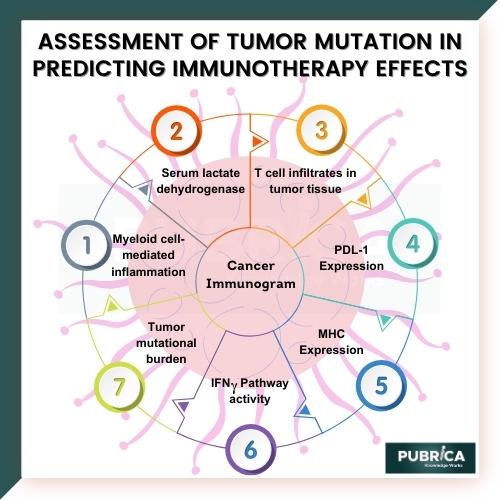
مواد و روش ها:
- بررسی ادبیات: ما به طور سیستماتیک مطالعات و کارآزمایی های بالینی موجود را که رابطه بین TMB و پاسخ ایمونوتراپی را بررسی کرده اند، مرور خواهیم کرد. مطالعاتی که معیارهای ورود از پیش مشخص شده را برآورده میکنند برای متاآنالیز در نظر گرفته میشوند.
- بازیابی دادهها: دادههای مربوط به سطوح TMB، نتایج ایمونوتراپی و سایر پارامترهای مرتبط از مطالعات انتخاب شده استخراج خواهد شد.
- متاآنالیز: تجزیه و تحلیل آماری برای ارزیابی اندازه اثر کلی TMB بر پاسخ ایمونوتراپی انجام خواهد شد. تجزیه و تحلیل های زیر گروه بر اساس نوع سرطان و رویکرد ایمونوتراپی انجام خواهد شد.
- ارزیابی بیوانفورماتیک: ما در مقیاس تجزیه و تحلیل خواهیم کرد ژنومی مجموعه دادهها برای بررسی مکانیسمهای مولکولی نهفته در رابطه بین TMB و پاسخ ایمنی درمانی. این شامل بررسی ریزمحیط تومور، نفوذ سلول های ایمنی و بار نئوآنتی ژن است.
- یکپارچه سازی یافته هانتایج متاآنالیز و یافته های بیوانفورماتیک برای ارائه یک ارزیابی جامع از ارزش پیش آگهی TMB در زمینه ایمونوتراپی ادغام خواهند شد.
معیارهای انتخاب
این مطالعه از معیارهای ورود به مطالعه استفاده کرد:
- همه بیماران مبتلا به سرطان تشخیص داده شدند و TMB بر اساس بافت تومور تشخیص داده شد.
- حداقل یک داده ORR، DCB، OS و PFS ممکن است در دسترس باشد.
- حجم نمونه بیشتر از 20 بود.
- مطالعات در مورد غیر مترادف جهش ها همچنین به دلیل سازگاری اصل اندازه گیری گنجانده شدند.
- بیماران تحت درمان با تک درمانی ICI. از سوی دیگر، مطالعاتی که هر یک از موارد زیر را برآورده می کنند.
معیارها حذف شدند:
- TMB از DNA یا خون تومور در گردش تشخیص داده می شود.
- تعریف TMB بالا و TMB پایین واضح نبود و همچنین TMB از a مشتق نشده بود مدل یادگیری ماشینی.
- حجم نمونه کمتر از 20 است یا رویدادهای اصلی مشاهده شده را نمی توان به دست آورد.
- بیمارانی که تحت درمان با ICI قرار نگرفته اند یا به طور همزمان درمان دیگری غیر از ICI دریافت کرده اند.
- مطالعات غیر انسانی، چکیده کنفرانس، بررسی، فراتحلیل، تفسیر یا نامه.
استخراج داده ها و ارزیابی کیفیت
دو محقق مستقل (CJL، YX) عناوین و چکیده مقاله را ارزیابی کردند و مطالعاتی که معیارهای انتخاب را داشتند برای ارزیابی متن کامل بازیابی شدند. یک ارزیابی کیفی از ادبیات نیز در طول انجام شد بازیابی دادهها. محقق سوم (CSY) به حل چند تناقض کمک کرد. نویسنده اول، سال انتشار، کشور مورد مطالعه، نوع مطالعه، نوع سرطان، مرحله سرطان، داروی ایمونوتراپی، هدف دارو، روش تشخیص TMB، قطع TMB، تعداد بیماران با TMB بالا/پایین، و دادههای مرتبط برای DCB، ORR، OS، و PFS در یک صفحه گسترده اکسل استخراج شد.
تجزیه و تحلیل بیوانفورماتیک
ما داده های تغییرات نوکلئوتیدی ساده (SNV) را از پایگاه داده TCGA به دست آوردیم (https://portal.gdc.cancer.gov/). نوع گردش کار MuTect2 Variant Aggregation and Masking و فرمت داده ها maf بود. سپس TMB هر نمونه با استفاده از برنامه Maftools R محاسبه شد. تجزیه و تحلیل Kaplan-Meier از بقای کلی با استفاده از نرم افزار R و Log-Rank برای آزمایش TMB 33 تومور با سطح برش 70٪ انجام شد. نتایج تجزیه و تحلیل KM به عنوان یک قطعه جنگلی نمایش داده می شود.
تحلیل آماری
نرم افزار Stata 16.0 (Stata Corporation، College Station، TX، ایالات متحده) برای همه متاآنالیزها استفاده شد و ORR، DCB، OS و PFS بین گروه های TMB بالا و TMB پایین با استفاده از متاآنالیز مقایسه شد. برای DCB و ORR، RR > 1 نشان می دهد که گروه TMB بالا بر گروه TMB پایین برتری دارد. برای داده های ترکیبی HR و 95% CI OS/PFS، HR > 1 نشان می دهد که گروه TMB بالا نرخ بقای بدتری نسبت به گروه TMB پایین دارد. زمانی که I2 بیشتر از 50% باشد از مدل اثر تصادفی و زمانی که I2 کمتر از 50% باشد از مدل اثر ثابت استفاده می شود. ما همچنین تجزیه و تحلیل زیر گروهی از OS و PFS را برای انواع مختلف تومور، مکانها و تکنیکهای تشخیص TMB انجام دادیم.
بحث
انتظار میرود که نتایج این مطالعه، کاربرد پیشآگهی TMB را روشن کند نشانگر زیستی برای اثرات ایمنی درمانی در درمان سرطان. درک مکانیسمهای مولکولی و عوامل مؤثر بر تأثیر TMB بر پاسخ ایمنی درمانی به توسعه استراتژیهای درمانی شخصی کمک میکند و ممکن است به اصلاح معیارهای انتخاب بیماران برای ایمونوتراپی کمک کند.
نتیجه
ادغام روش های متاآنالیز و بیوانفورماتیک بینش ارزشمندی را در مورد نقش TMB در پیش بینی اثرات ایمونوتراپی ارائه می دهد. این تحقیق پتانسیل پیشرفت زمینه ایمونوتراپی سرطان و بهبود نتایج بیمار را با هدایت تصمیمات درمانی بر اساس شدت جهش تومور دارد. اگرچه مطالعات بیشتری برای ایجاد رویکرد بهینه برای استفاده از TMB در عمل مورد نیاز است، این نتایج تأیید میکند که TMB یک نشانگر زیستی پیش آگهی امیدوارکننده است که میتواند پاسخ بیوانفورماتیک بالینی و نتیجه پیش آگهی ایمونوتراپی را پیشبینی کند. بنابراین، یافته های ما از TMB بالا به عنوان یک نشانگر زیستی درمانی که ممکن است مدیریت ایمنی درمانی سرطان را بهبود بخشد، پشتیبانی می کند.
ما را بررسی کنید مثال ها برای درک سازگاری ما با موضوعات و حوزه های موضوعی آمار زیستی.
منابع
- ساساکی، هیرونوبو و همکاران. “دیابت نوع 1 جدید به دنبال واکسیناسیون علیه بیماری کروناویروس 2019: گزارش یک مورد.” مجله بررسی دیابت 13.6 (2022): 1105-1108.
- یانو، ماساهیرو و همکاران “دیابت نوع 1 جدید به دنبال واکسیناسیون mRNA COVID-19.” داخلی 61.8 (2022): 1197-1200.
- ساکورای، کاناکو و غیره “دیابت نوع 1 پس از واکسن مبتنی بر RNA علیه کووید-19.” مجله تحقیقات دیابت 13.7 (2022): 1290-1292.