استفاده از حیوانات در تحقیقات علمی مدتی است که موضوعی بحث برانگیز بوده است. هنوز نظرات متفاوتی در مورد تحقیقات حیوانی وجود دارد و بسیاری از مردم بر این باورند که حیوانات نه تنها برای بهبود درک ما از بیماریهای پیچیده مانند سرطان، بلکه برای آزمایش داروها و لوازم آرایشی گزینه مناسبی هستند. با این حال، بسیاری از مردم استدلال می کنند که استفاده از حیوانات غیراخلاقی، بی رحمانه و غیر ضروری است.
تنها در بریتانیا، استفاده از حیوانات در سال 2021 تا 6 درصد افزایش خواهد یافت. با پیچیدهتر شدن بیماریها و افزایش تقاضا برای تحقیقات نوآورانه، این احتمال افزایش مییابد. در یک دنیای ایده آل، ما اصلاً مجبور نیستیم برای تحقیق به حیوانات آسیب برسانیم، بنابراین در حال حاضر چه گزینه های دیگری داریم؟
رشد سلول ها به صورت سه بعدی واقعاً بسیار سخت است…
«خطوط سلولی» ساخت بشر معمولاً ساده ترین و قابل اعتمادترین گزینه برای مطالعه بیماری های انسانی یا آزمایش داروهای جدید است. آنها در ابتدا از نمونههای بافت سالم یا ناسالم اهدایی بیماران با رضایت استخراج میشوند و سپس منجمد، ذخیره میشوند و بارها و بارها برای آزمایش استفاده میشوند. اگرچه آنها یک مدل زنده برای آزمایش ارائه می دهند، اما هنوز در هنگام بررسی بیماری های پیچیده یا تداخلات دارویی با ایده آل فاصله دارند. خطوط سلولی فقط در یک لایه دوبعدی در ته پتری دیش رشد می کنند، نه به صورت سه بعدی مانند یک اندام زنده واقعی. به همین دلیل، آنها همچنین به ترتیب عجیبی رشد می کنند – روی هم، وارونه یا پشت به جلو، که در بدن اتفاق نمی افتد. یکی دیگر از مضرات این مدلهای ساده این است که در هر بار فقط یک نوع سلول در ظرف رشد میکند، به این معنی که آنها فوقالعاده ابتدایی هستند و نتیجهگیری محکمی از آنها بدون تکرار آزمایشهای مشابه با سایر انواع سلول دشوار است.
مدل سازی یک قطعه از بافت زنده یا یک عضو کامل بدون توسل به کار حیوانات کار دشواری است. در طول دهه گذشته، داربست های مهندسی شده یا مبتنی بر گیاه در بین دانشمندان و محققان رایج شده اند که می توانند در سلول ها محصور شوند و مانند یک اندام زنده مورد مطالعه قرار گیرند. داربست های گیاهی از مواد طبیعی مشتق شده اند که برای تعامل و تقویت رشد سلول های زنده طراحی شده اند. بسیاری از مواد طبیعی آزمایش و آزمایش شدهاند، اما برخی از جالبترین آنها شامل آلژینات (جلبک دریایی)، نشاسته (گیاهان) و سلولز است که میتوان آنها را از سیب برداشت کرد. ایده کلی این است که این مواد استریل می شوند، آماده می شوند و سپس سلول ها را می توان در یک لایه 2 بعدی بر روی آنها بذر کرد. سلول ها زمانی بسیار خوشحال تر می شوند که بتوانند بر روی یک سطح مناسب بر خلاف پتری دیش رشد کنند! کاربردهای مختلفی برای این فناوری وجود دارد، مانند استفاده از داربست های گیاهی برای تولید تعداد زیادی سلول که می توانند برای آزمایش های بعدی مانند آزمایش دارو مورد استفاده قرار گیرند. علاوه بر کارهای آزمایشگاهی، پتانسیلی برای استفاده از این فناوری سلول به اضافه داربست در پزشکی وجود دارد، مانند جایگزینی برای پیوند پوست. متأسفانه، این نوع کاربرد هنوز در حال تحقیق است زیرا عوامل زیادی مانند واکنش آلرژیک، التهاب و رد شدن باید در نظر گرفته شوند. فقط به این دلیل که یک ماده در آزمایشگاه رفتار خاصی دارد، وقتی وارد بدن می شود می تواند کاملاً متفاوت رفتار کند و حتی از بین برود یا بیشتر از اینکه مفید باشد باعث آسیب شود.
اگر سلولهای طبیعی برای مطالعه بیماریهای دشوار، حتی زمانی که روی داربست رشد میکنند، بسیار ابتدایی میشوند، آیا میتوان به جای آن یک عضو فعال را رشد داد؟

کشف ارگانوئید
این یک سوال خاص است که مدتی است ذهن بسیاری از مردم را درگیر کرده است و معلوم است که پاسخ آن بسیار پیچیده تر از آن چیزی است که ما فکر می کنیم.
در حال حاضر، روشهایی برای رشد اندامهای با عملکرد کامل از ابتدا در آزمایشگاه هنوز کشف نشده است. در عوض، “ارگانوئیدها” به مدل های محبوب در تحقیقات آزمایشگاهی تبدیل شدند. اندامک ها در نیمه راه بین خطوط سلولی و کل اندام های فعال قرار دارند. آنها بسیار کوچک، گرد هستند و از سلول های بنیادی پرتوان القایی (iPSCs)، سلول های بنیادی جنینی (ESCs) و حتی بیماران سالم یا سرطانی مشتق از سلول های بنیادی بالغ منشاء می گیرند. اما چگونه دانشمندان متوجه شدند که چگونه سلول های بنیادی را به ارگانوئید تبدیل کنند؟
ژنتیک مولکولی هلندی و برنده جایزه Keio برای علوم پزشکی هانس کلورز و تیمش در موسسه هوبرشت اولین افرادی در جهان بودند که در مطالعه ارگانوئیدها پیشگام شدند. در سال 2008، کلورز این فرضیه را مطرح کرد که می تواند از بافت بیوپسی روده برای به دست آوردن سلول های بنیادی استفاده کند، که سپس می تواند برای تولید سلول های بنیادی بیشتر استفاده شود. اتفاقی که در واقع اتفاق افتاد پیشگامانه بود. نه تنها سلول های بنیادی بیشتری همانطور که او انتظار داشت تشکیل شد، بلکه گروهی از سلول ها در ظرف پتری شبیه بافت اولیه بودند و بیشتر شبیه روده کوچک شدند! این تولد اولین ارگانوئید بود.
از زمان این کشف، چندین محقق روش های توسعه یافته توسط Clevers را امتحان کرده اند. هم بافت سالم و هم بیمار را می توان، معمولاً با بیوپسی، از بیماران مختلف با رضایت جمع آوری کرد، که بعد از عمل به خانه می روند و روز خود را ادامه می دهند. سپس این بافت به آزمایشگاه منتقل میشود، جایی که پروتکلهای پیچیده برای استخراج سلولهای بنیادی و تبدیل آنها به ارگانوئیدها انجام میشود.
ارگانوئیدهای “سفارشی” رشد یافته در آزمایشگاه
ارگانوئیدها نیز به روده محدود نمی شوند، زیرا محققان با موفقیت ارگانوئیدهای معده سالم مشتق شده از بیمار را توسعه داده اند. سپس از این ارگانوئیدها می توان در آزمایشگاه برای مدل سازی پوشش معده استفاده کرد، به عنوان مثال برای شبیه سازی زخم معده یا توسعه سرطان. بافت ناسالم بیمار مانند تومورها نیز به ارگانوئیدهای تومور مشتق شده از بیمار (PDTOs) تبدیل می شوند که به عنوان توموروئیدها نیز شناخته می شوند، از جمله سرطان سینه، سرطان کولورکتال، کبد، مغز و پانکراس. توموروئیدها به ویژه یک پیشرفت بزرگ در تحقیقات سرطان هستند زیرا به دانشمندان اجازه می دهند تومورهای خارج از بدن را بررسی و مطالعه کنند. برای مثال، سیگنالدهی سلولی و تداخلات با داروهای ضد سرطان یا شیمیدرمانی را میتوان بدون نیاز به آزمایش روی بیمار یا تولید مثل در حیوانات به طور گسترده مشاهده کرد.
کاربردها و انواع تحقیقات زیادی وجود دارد که از ارگانوئیدها علاوه بر کشف دارو و مدل سازی بیماری استفاده می کنند. برنامه های اضافی در تصویر زیر نشان داده شده است.
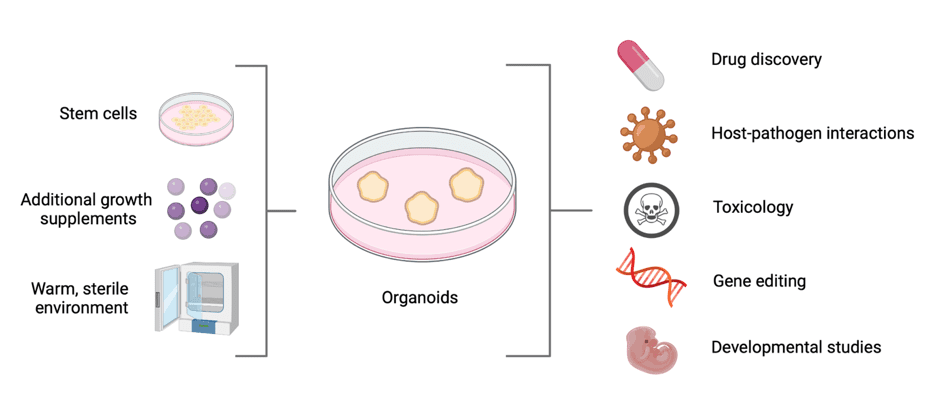
ارگانوئیدهای مشتق شده از انسان دنیایی از امکانات را برای دانشمندان و محققان به طور یکسان گشوده است. آنها یک مدل ایده آل برای انجام تعدادی آزمایش بدون نیاز به آسیب رساندن به حیوان ارائه می دهند. ارگانوئیدها به حل مشکل مرتبط با رده های سلولی دو بعدی کمک می کنند زیرا انواع مختلفی از سلول ها را ارائه می دهند در حالی که هنوز تا حدودی شبیه بافت یا اندام اصلی هستند. به عنوان مثال، این بدان معناست که محققان مجبور نیستند برای رسیدن به نتیجه، دارو یا تکنیک مشابهی را در هر زمان روی چندین رده سلولی مختلف آزمایش کنند. ارگانوئیدها همچنین دریچه ای را برای “پزشکی شخصی” باز کرده اند – اگر ارگانوئیدهای مشتق شده از بیمار به داروها در آزمایشگاه پاسخ دهند، آیا به این معنی است که آن داروها را می توان با خیال راحت به بیمار داد؟ ما هنوز با این نتیجه گیری فاصله داریم، زیرا ارگانوئیدها هنوز سیستم های نسبتا ساده ای هستند، اما ممکن است در آینده جایگزین نیاز به آزمایش های بالینی گسترده و پرهزینه شوند.
در حالی که امیدوارکننده است، شایان ذکر است که ارگانوئیدها فاقد بسیاری از ویژگیهایی هستند که ما در بدنمان بدیهی میدانیم، مانند سیستم گردش خون، تنفس و سیستم ایمنی. در حال حاضر، اکثر مطالعات ارگانوئیدی این عوامل را در نظر نمیگیرند، که نتیجهگیری را محدود میکند. مشکل دیگر اندازه ارگانوئیدها است، زیرا معمولاً قطر آنها از 1 میلی متر بیشتر نیست. از آنجایی که آنها بسیار مینیاتوری هستند، کار با آنها دشوار است و نیازهای پیچیده ای برای رشد و نگهداری دارند.
در نهایت، ما هنوز با حذف کامل استفاده از حیوانات در تحقیقات فاصله داریم، اما ارگانوئیدها چشم انداز هیجان انگیزی برای آینده تحقیقات بیولوژیکی هستند و قطعاً گامی در مسیر درست هستند.
پیام ارگانوئیدها: جایگزین های بدون حیوانات در تحقیقات پزشکی اولین بار در ظاهر شد شورای علمی ایلینوی.

